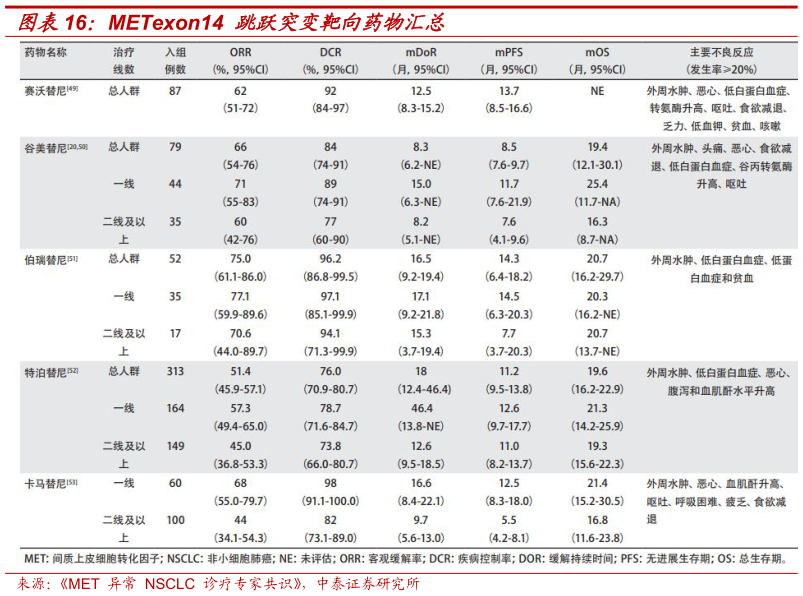
> 数据图表一起讨论下METexon14 跳跃突变靶向药物汇总
2025-4-3 赛沃替尼 MET exon14 患者临床数据优异,2021 年获附条件批准上市,2025 年 1 月获批转为常规批准,涵盖初治、经治患者。中国人群的METexon14 跳跃突变的发生率为 0.9%-2.0%,在肺腺癌患者中的发生率较高,约为 3%,在肺鳞癌患者中发生率为 1%-2%。METexon14 跳跃突变患者的肿瘤细胞具有高度侵袭性,往往在抗肿瘤治疗过程中出现耐药性且预后不良,无论是一线化疗还是免疫治疗的疗效均不太理想。赛沃替尼早前已于 2021 年 6 月基于 II 期临床结果在中国获附条件批准,用于治疗接受全身性治疗后疾病进展或无法接受化疗的 MET 外显子 14 跳变的非小细胞肺癌患者,是中国首个获批的选择性 MET 抑制剂,并自 2023 年 3 月起纳入国家医保药品目录。2024 年欧洲肺癌大会(ELCC)公布一项赛沃替尼治疗 MET ex14 跳突 NSCLC 患者的b 期确证性研究结果,截至 2023 年 10 月 20 日,初治、经治患者的 ORR 分别为 62.1% 和 39.2%,DCR 分别为 92.0% 和 92.4%此外,初治患者的 mPFS 为 13.7 个月,mOS 尚未达到经治患者的 mPFS为 11.0 个月,mOS 未成熟。基于该数据的公布,赛沃替尼是国内目前唯一有 IIIb 期确证性研究数据的 MET 抑制剂,临床结果获国家卫健委、中国临床肿瘤学会、中国抗癌协会、中华医学会、中国胸部肿瘤研究协作组等多机构指南认可。2025 年 1 月,赛沃替尼用于治疗 MET 外显子 14 跳变的局部晚期或转移性非小细胞肺癌成人患者的新适应症上市申请已取得中国国家药品监督管理局 国家药监局 批准,早前沃瑞沙在经治患者中的附条件批准转为常规批准,沃瑞沙在中国的新适应症将扩展至同时涵盖初治和经治患者。