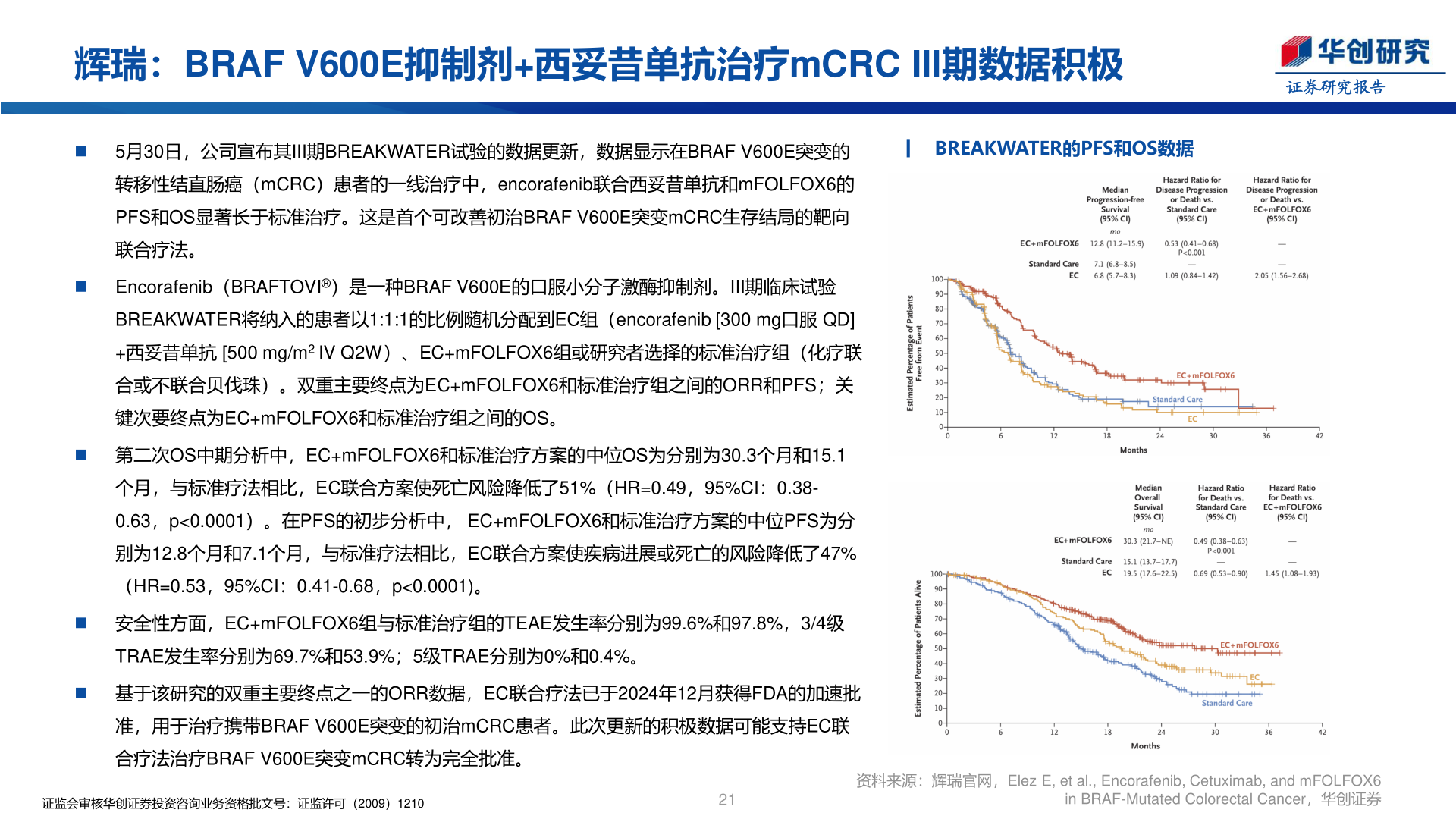
> 数据图表如何了解辉瑞:BRAF V600E抑制剂+西妥昔单抗治疗mCRC III期数据积极
2025-6-1