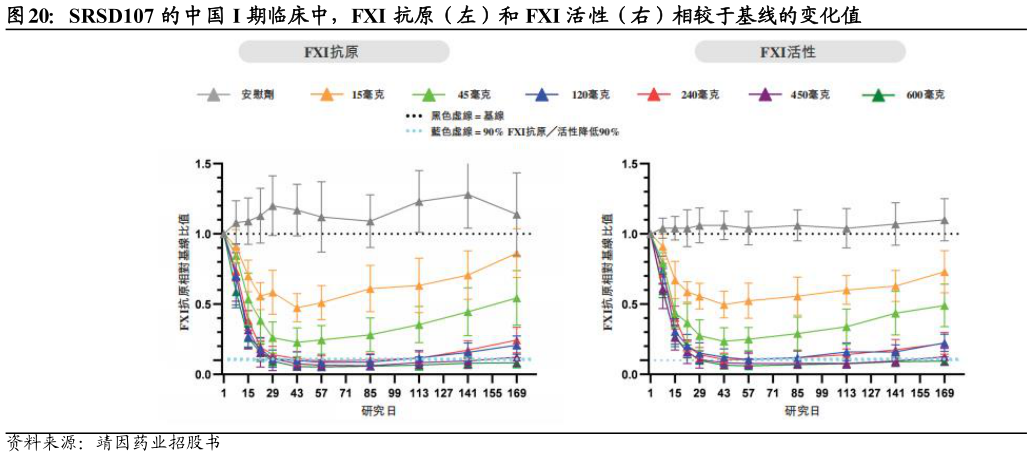
> 数据图表如何解释SRSD107 的中国 I 期临床中,FXI 抗原(左)和 FXI 活性(右)相较于基线的变化值
2026-2-3瑞博生物于 2024 年 8 月在瑞典启动 RBD4059 的 IIa 期临床试验,旨在评估在患有稳定型冠状动脉疾病参与者中,RBD4059 的安全性、药代动力学和药效学,安慰剂组为标准治疗加低剂量阿司匹林。该试验已于 2025 年 2 月完成了患者入组。 2.4.2 SRSD107:牵手 CRISPR 出海,计划推进多个适应症 SRSD107 是靖因药业开发的靶向 FXI 的 siRNA 药物,其差异化特性在于潜在地结合了卓越的出血安全性、卓越的给药频率、更长的有效时间,以及治疗目前不适用于 DOAC 高危患者群体和接受 DOAC 治疗但需要调整剂量的患者。靖因药业计划将 SRSD107 推进至多个适应症,包括未治疗的新房颤动、癌症相关血栓形成、慢性肾病、外周血管疾病、慢性冠状动脉疾病及缺血性卒中预防及静脉血栓栓塞等现有疗法不充分或存在治疗禁忌的 适应症。 2025 年 5 月,靖因药业就 SRSD107 和 CRISPR Therapeutics 建立了全球 50:50 的共同开发及商业化合作推进的协议,基于此,靖因药业预先获得了 25百万美元的现金及价值约 70 百万美元的 CRISPR 股票,并有资格获得超过800 百万美元的里程碑付款,及可能授权给 CRISPR 的产品的未来特许权使用费。 临床 I 期结果证明 SRSD107 可剂量依赖性地持续、显著降低 FXI 水准,同时使活化部分凝血活酶时间延长。在澳大利亚和中国开展的 I 期试验中,SRSD107 表现出高达 95%的循环 FXI 水平的降低,作用时间持续 6 个月,且 aPTT 相应延长 2.4 倍,证实了其对内源性通路的有效抑制。该疗法耐受性良好,未发生严重不良事件,表明其相较于传统抗凝药物具备在降低血栓风险的同时最大限度减少出血并发症的潜力。